分子栄養学「赤血球の『ヘム』生合成に必要な栄養素(ビタミンB6・亜鉛・鉄)」
私たちが呼吸によって取り入れる酸素は、体内でエネルギーを作るために欠かせない物質です。
そしてその酸素を全身に届けているのが「赤血球(せっけっきゅう)」という細胞であり、実際にその酸素をギュッとつかまえる役割を担っているのが、赤血球のヘモグロビンに含まれる「ヘム」という分子です。
今回は、ヘムを合成するために必要な栄養素(ビタミンB6・亜鉛・鉄)について解説いたします。
「ヘム」の正体とは?
まず、ヘムとは何かを見ていきましょう。
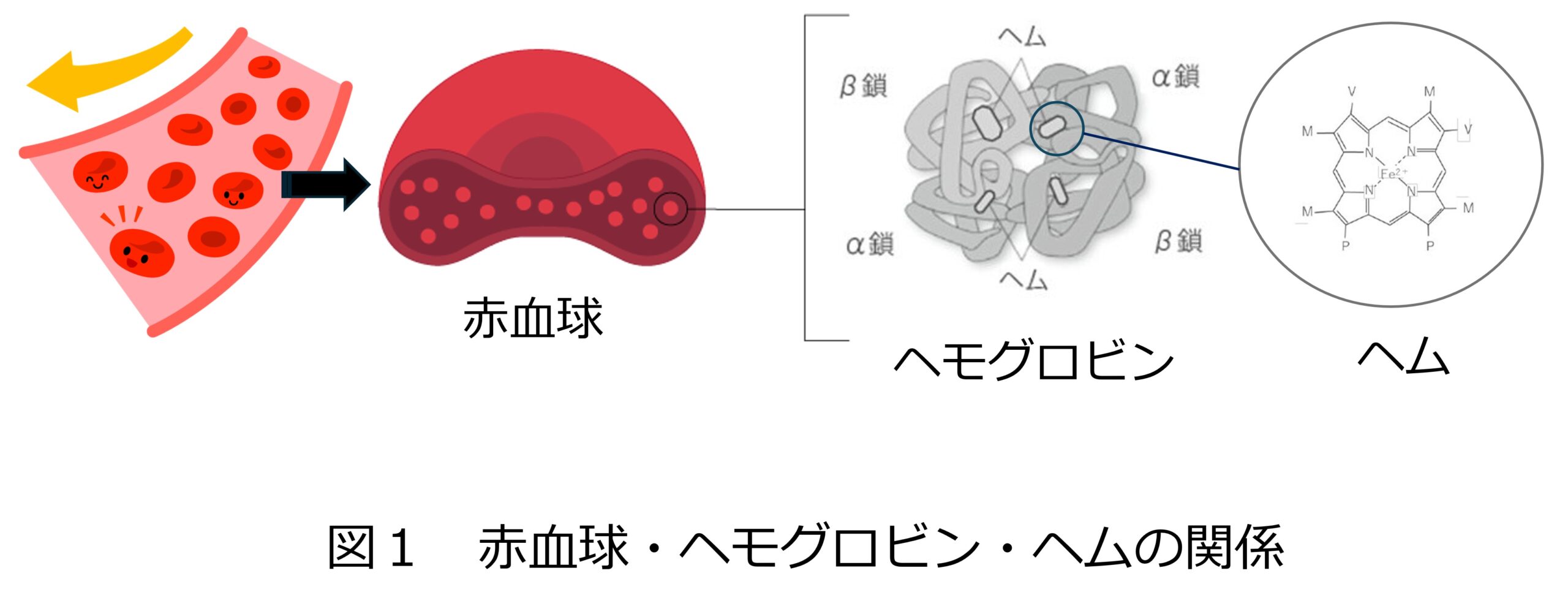
血管を流れて酸素を運ぶ赤血球。赤血球1個の中には「ヘモグロビン」というタンパク質が大量に詰まっており、赤血球1個の約1/3の濃度を占めています。
そしてそのヘモグロビンの中に存在し、実際に酸素をつかまえる役割を担っているのが「ヘム」という物質です※1(図1)。
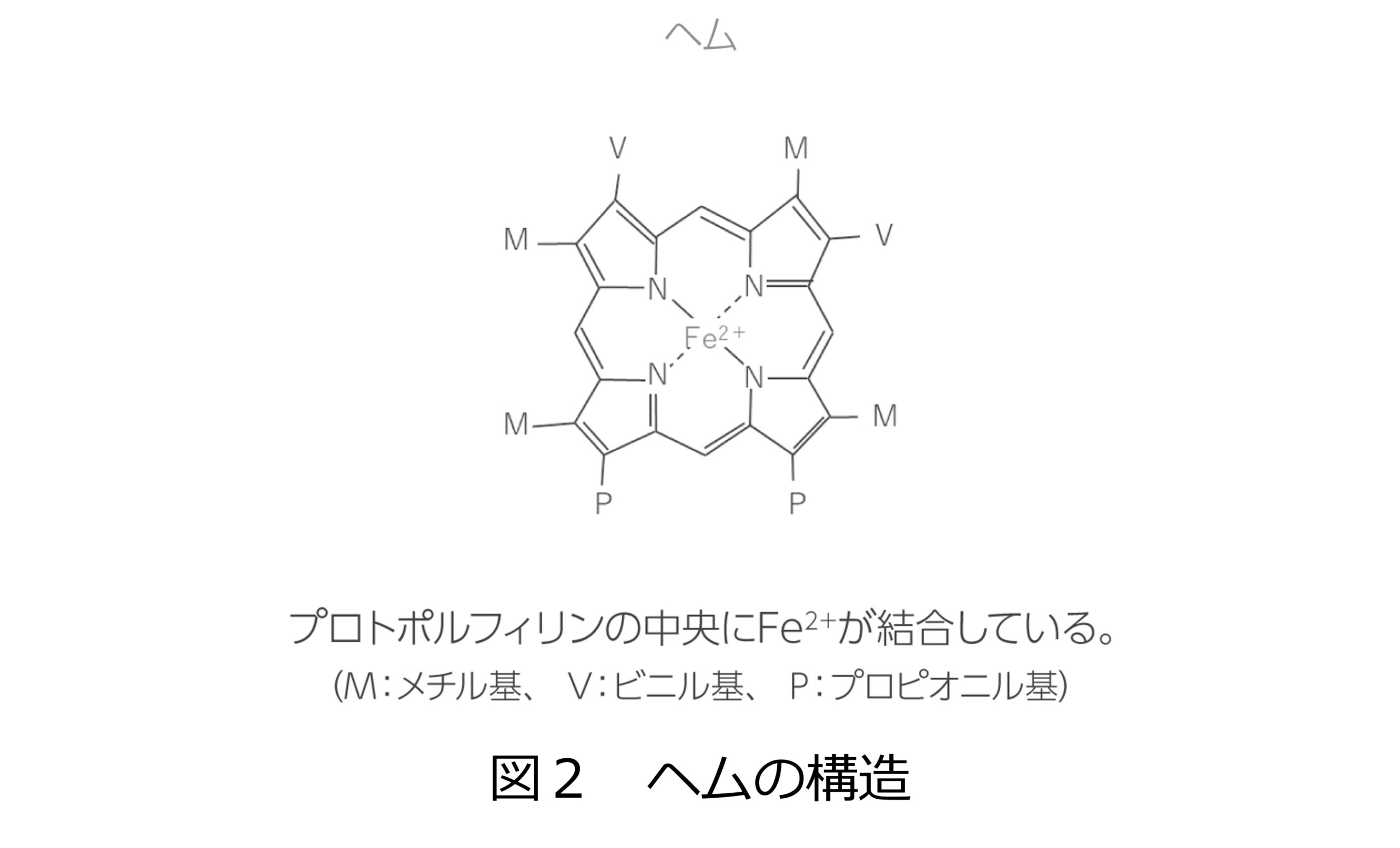
ヘムは鉄と「プロトポルフィリン(protoporphyrin)」という環っか状の構造が合体してできた分子であり※2、※3(図2)、体内に存在する鉄の大部分はヘムとして存在しています※4。
ヘムは以下のような、生命維持に欠かせない場所で働いています※5。
・血液中での酸素の運搬
・筋肉における酸素の貯蔵
・細胞の中でエネルギーを作るミトコンドリア(細胞の中にある小さな発電所のような細胞内小器官)での機能
・薬などを解毒する肝臓の酵素 など
ヘムはどこで合成される?
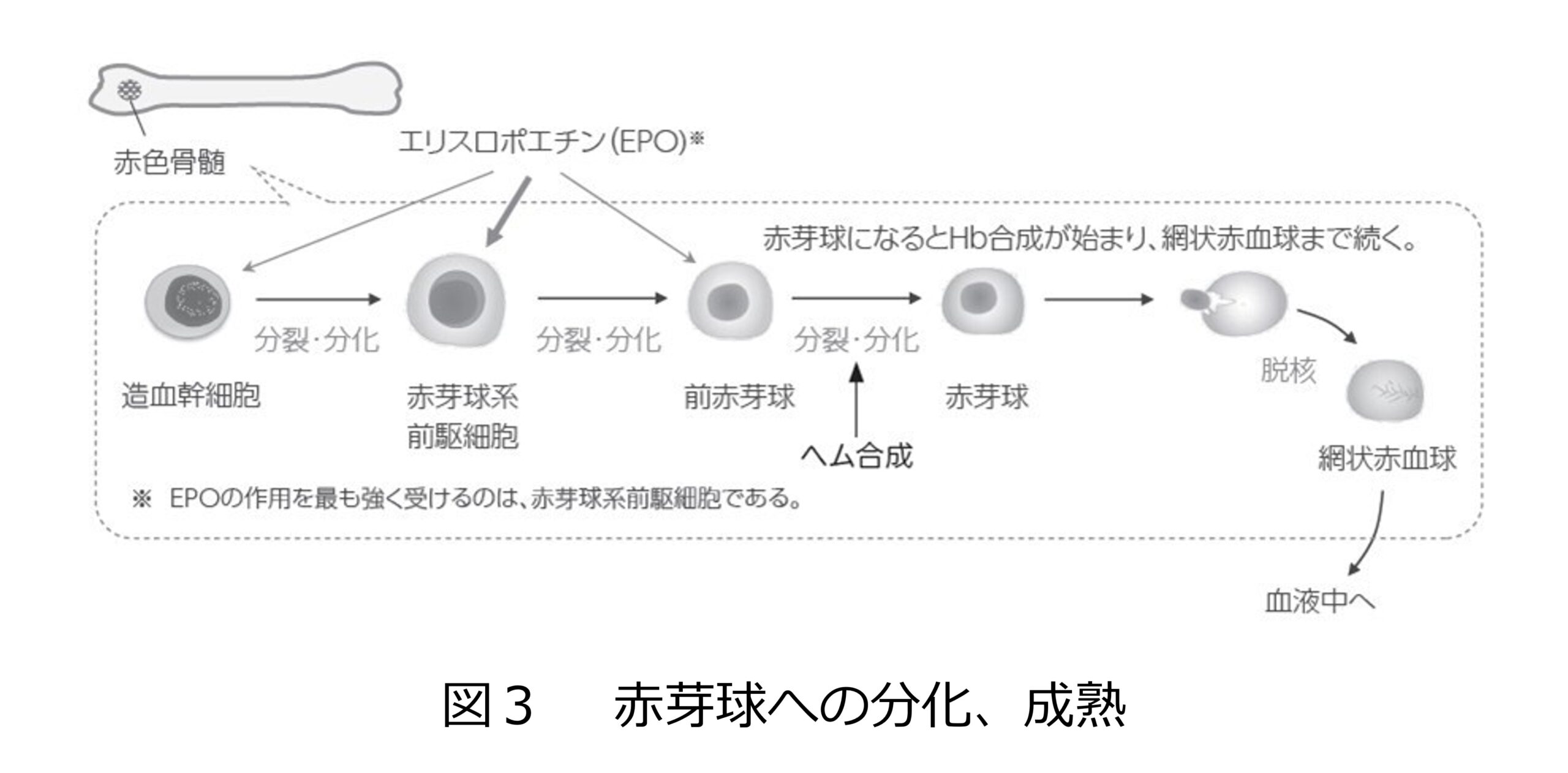
ヘムの生合成は、ミトコンドリアをもち、ヘムをつくる能力をもつすべての細胞で行われます。最も多く合成されるのが骨髄(赤芽球)、次いで肝臓での合成が活発であると報告されています※5、※6。
赤芽球とは、成熟した赤血球になる前の段階にある、分化途中の幼若な赤血球のことです。赤血球系細胞におけるヘム生合成は赤芽球で始まり、網状赤血球まで続くことが報告されています※7(図3)。
ヘム生合成「8段階の物語」に必要な栄養素(ビタミンB6・亜鉛・鉄)
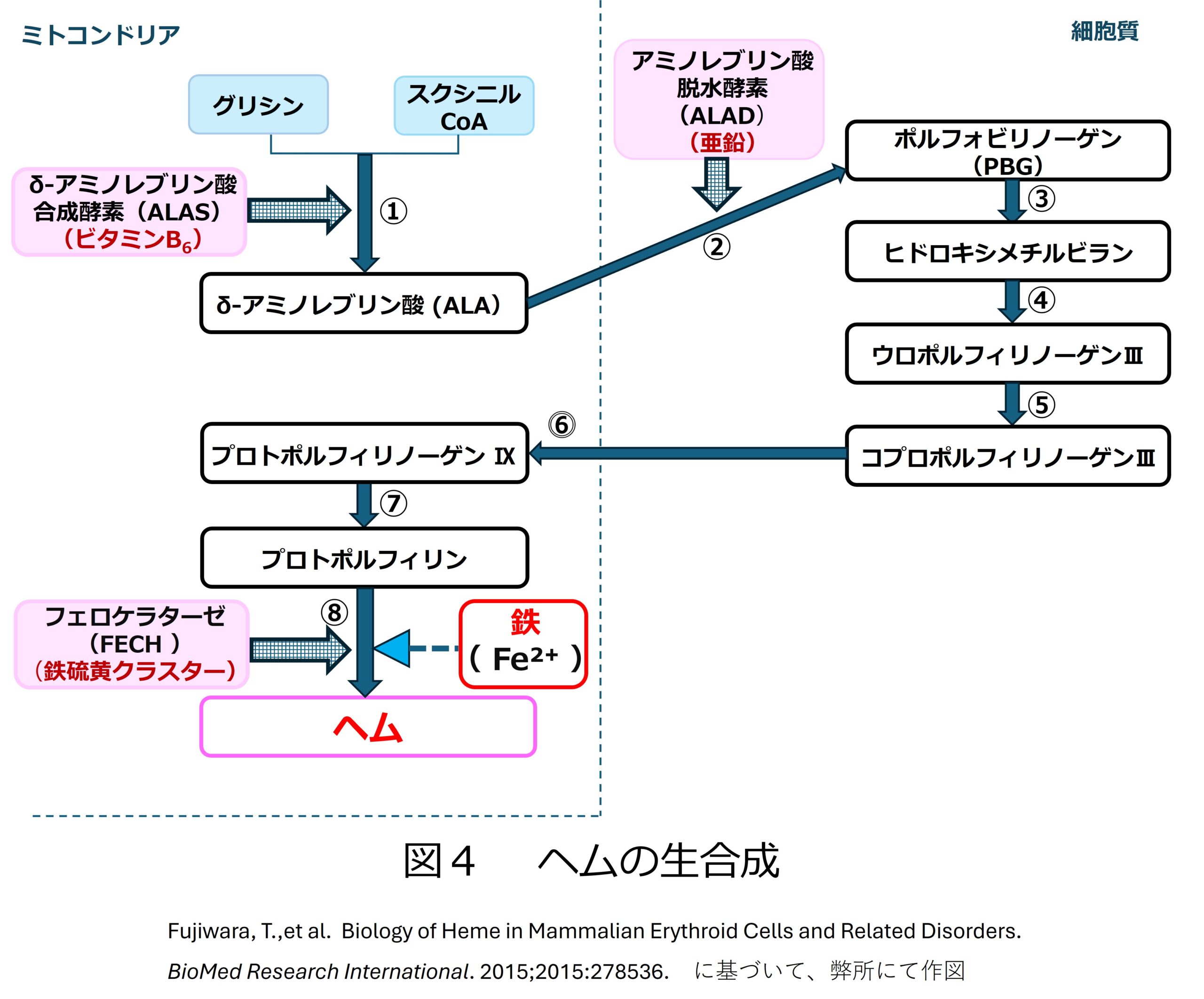
ヘムが完成するまでの過程は、それぞれの細胞内の2つの場所(ミトコンドリアと細胞質)をまたぎ、全8段階(以下①~⑧)の精密な酵素反応を経て進みます(図4)※5、※8、※9。
以下、その流れを順に見ていきましょう。下記①・⑥~⑧はミトコンドリアで、②~⑤が細胞質で行われます※10。
①スタート: ミトコンドリア内で、アミノ酸の一種である「グリシン」と、「スクシニルCoA」が合体し、δ-アミノレブリン酸 (ALA)がつくられます。この反応には、δ-アミノレブリン酸合成酵素(ALAS)(補酵素:ビタミンB6)が必要です※11、※12、※13。
↓
②細胞質へ移動: 作られたALAは一旦ミトコンドリアの外(細胞質)へ出ます。ここで2分子のALAがくっつき、ポルフォビリノーゲン(PBG)になります。この反応には、アミノレブリン酸脱水酵素(ALAD)(補因子:亜鉛)が必要です※12、※14、※22。
↓
③④⑤PBGが4つつながって一本の鎖のようになり(ヒドロキシメチルビラン)、その鎖がくるりと輪っか状に閉じます(ウロポルフィリノーゲンIII)。そして輪っかの周りについている余分な飾りを外して形を整え(コプロポルフィリノーゲンⅢ)、また再びミトコンドリアの中に入ります。
↓
⑥⑦ミトコンドリア内でさらに形が整えられ(プロトポルフィリノーゲン Ⅸ)、さらに水素が除かれるなどしてヘムの一歩手前の姿(プロトポルフィリン)になります。
↓
⑧ゴール(鉄が納まる): 最後にプロトポルフィリンの中心部へ「鉄」をパチッとはめ込んで、ついに「ヘム」が完成します。この反応を触媒する酵素フェロケラターゼ(FECH)には、鉄硫黄クラスターが存在します。この鉄硫黄クラスターの働きは不明との報告もあり※12、その機能が研究されています※12、※15、※16。
「補酵素・補因子」という名の助っ人たち
この8段階の反応がスムーズに進むためには、ビタミンB6・亜鉛・鉄の3つの栄養素が不可欠です。
補酵素(ほこうそ)・補因子(ほいんし)とは、酵素が働くために必要なサポート役のようなものです。補酵素・補因子を必要とする酵素は、これらが不足すると働きを発揮できなくなります。
体内で毎日休みなく繰り返されるこの8段階のリレーは、ビタミンB6・亜鉛・鉄の力を借りて進めることのできる、まさに健康を支える生命の基礎となります。
赤血球のヘムをつくるための鉄はどこから補給される?
健康な人の体内では、毎日約2,000億個もの赤血球が新たに産生されています※17。これに必要な鉄の大部分は、体内での鉄のリサイクルによって賄われています。
健康な赤血球の寿命は約120日ですが、寿命を終えた赤血球から回収された鉄は積極的に体外に排泄されることなく、新しい赤血球の生成などに再利用されます。
一方で、健康な人でも毎日約1mgほどの鉄が消化管粘膜や皮膚の剥がれ落ちなどによって生理的に失われることが示されています※18。
これを補うのが、日々の食事から摂取する鉄です。バランスのよい1日3食の食事からの鉄の吸収率を約10%とすると、実際に体に取り込まれる量は約1mg程度となり、これがほぼ1日の損失分(約1mg)を補う計算になります。
「貯蔵鉄」という人体の”鉄の貯金”
補給が追いつかない場合、まず「貯蔵鉄」が使われます。貯蔵鉄とは、いわば人体における「鉄の貯金」です。生物学的に利用されなかった余剰な鉄はフェリチンなどとして貯められ※19、体内で鉄が足りないときには、ここから鉄が供給されます※4。
鉄不足の状態が長期間続くと、貯蔵鉄が枯渇し、鉄欠乏が段階的に進行します※20。
1.まず貯蔵鉄が減少する
2.次に血清鉄が低下する
3.最終的にヘモグロビン鉄が減少し、WHOの定義する「貧血(ヘモグロビン濃度の低下した状態)」へと至る
「潜在性鉄欠乏(貧血を伴わない鉄欠乏)」の臨床的重要性
オーソモレキュラー分子栄養医学協会が提唱する血液データ解析に基づく個別化栄養療法「金子メソッド」では、血清フェリチン値を重要な指標のひとつに位置づけています※21。
特に注目すべきは、ヘモグロビン低下(貧血)として現れる前の段階、すなわち血清フェリチン値の低下などで検出される「潜在性鉄欠乏(貧血を伴わない鉄欠乏)」においても、多くの未診断症状が生じる可能性があるという点です※21。
まずは自分の身体の状態を「金子メソッド」という客観的な指標で確認し、医師とともに健康維持・増進への第一歩を踏み出してみませんか。
金子メソッドは、倦怠感など未病の状態に悩む多くの無症候性・未診断の患者さんを救う可能性を秘めた、新しい栄養療法であると報告されています※21。
(※金子メソッド(Kaneko’s method)とは?血液データ解析に基づく個別化栄養療法)
※1 Marengo-Rowe, AJ. Structure-function relations of human hemoglobins. Proceedings (Baylor University. Medical Center). 2006;19(3):239-245.
※2 プロトポルフィリンはポルフィリンの一種で、ヘムの前駆物質です。プロトポルフィリンⅨともいいます。プロトポルフィリンⅨの中央に鉄が納まることで、ヘムが出来上がります。
※3 ポルフィリンとは、4個のピロールと呼ばれる窒素を1つ含む五員環化合物が、4個の炭素原子と結合した環状化合物の総称です。
※4 Dutt, S.,et al. Molecular mechanisms of iron and heme metabolism. Annual Review of Nutrition. 2022;42:311-335.
※5 Fujiwara, T.,et al. Biology of Heme in Mammalian Erythroid Cells and Related Disorders. BioMed Research International. 2015;2015:278536.
※6 Puy, H.,et al. Porphyrias. Lancet. 2010;375:924-937.
※7 Chiabrando, D.,et al. Heme and erythropoieis: more than a structural role. Haematologica. 2014;99(6):973-983.
※8 Phillips, JD. Heme biosynthesis and the porphyrias. Molecular Genetics and Metabolism. 2019;128(3):164-177.
※9 Belot, A.,et al. Update on heme biosynthesis, tissue-specific regulation, heme transport, relation to iron metabolism and cellular energy. Liver International. 2024;44(9):2235-2250.
※10 Dailey, HA.,et al. Erythroid heme biosynthesis and its disorders. Cold Spring Harbor Perspectives in Medicine. 2013;3(4):a011676.
※11 Astner, I.,et al. Crystal structure of 5-aminolevulinate synthase, the first enzyme of heme biosynthesis, and its link to XLSA in humans. EMBO Journal. 2005;24(18):3166-3177.
※12 Layer, G.,et al. Structure and function of enzymes in heme biosynthesis. Protein Science. 2010;19(6):1137-1161.
※13 ALASには、ミトコンドリアとヘム合成能力をもつすべての細胞に発現するALAS1と、赤血球特異的なALAS2の2つのアイソザイムがあり※9、どちらもPLP(ビタミンB6の補酵素型)を補酵素として必要とします※11。
※14 Jaffe, EK.,et al. The molecular mechanism of lead inhibition of human porphobilinogen synthase. Journal of Biological Chemistry. 2001;276(2):1531-1537.
※15 Crooks, DR.,et al. Posttranslational stability of the heme biosynthetic enzyme ferrochelatase is dependent on iron availability and intact iron-sulfur cluster assembly machinery. Blood. 2010;115(4):860-869.
※16 Schultz, IJ.,et al. Iron and porphyrin trafficking in heme biogenesis. Journal of Biological Chemistry. 2010;285(35):26753-26759.
※17 Muckenthaler, MU.,et al. A Red Carpet for Iron Metabolism. Cell. 2017;168(3):344-361.
※18 Green, R.,et al. Body iron excretion in man: a collaborative study. American Journal of Medicine. 1968;45(3):336-353.
※19 Mleczko-Sanecka, K.,et al. Cell-type-specific insights into iron regulatory processes. American Journal of Hematology. 2021;96(1):110-127.
※20 Berger, MM.,et al. ESPEN micronutrient guideline. Clinical Nutrition. 2022;41(6) 1357-1424.
※21 Arakaki, M.,et al. Personalized Nutritional Therapy Based on Blood Data Analysis for Malaise Patients. Nutrients. 2021; 13(10): 3641.
※22 2020年には、ALAD活性への鉄硫黄クラスターの関与を示す文献も登場しています※4、※23。
※23 Liu, G.,et al. Heme biosynthesis depends on previously unrecognized acquisition of iron-sulfur cofactors in human amino-levulinic acid dehydratase. Nature Communications. 2020;11(1):6310.